ㅇ 유효핵전하
: 바깥 전자 껍질에 채워진 전자가 실제로 받는 핵전하
Tip. 안쪽 전자 껍질에 채워진 전자들이 원자핵의 핵전하를 가림
Tip. 핵전하 : 원자핵이 가진 전하로 원자핵 내의 양성자 전하의 합과 같다.
|
|
1족
|
2족
|
13족
|
14족
|
15족
|
16족
|
17족
|
18족
|
|
2주기
|
Li
1.50
|
Be
2.05
|
B
2.70
|
C
3.20
|
N
3.85
|
O
4.55
|
F
5.20
|
Ne
5.80
|
|
3주기
|
Na
2.55
|
Mg
3.45
|
Al
4.05
|
Si
4.20
|
P
5.00
|
S
5.70
|
Cl
6.20
|
Ar
6.90
|
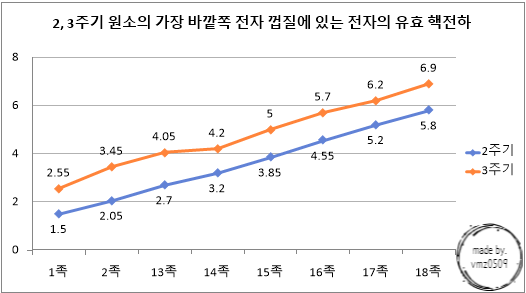
1. 가려막기 효과
: 다전자 원자에서 다른 전자들이 원자핵의 양전하를 가림으로써 전자가 느끼는 핵전하의 크기가 감소하는 효과
Tip. 단 수소는 전자가 1개이므로 가려막기 효과가 나타나지 않는다.
ㅇ 원자반지름
: 같은 종류의 두 원자가 화학 결합되어 있을 때 두 원자핵 사이의 거리의 반
Tip. 원자의 현대적 모형에서는 원자핵 주위에 존재하는 전자의 위치를 정확히 정의할 수 없다.
1. 비교순서
전자껍질 수
↓
유효핵전하
↓
전자사이 반발력
2. 원자에서
- 같은 주기에서는 원자 번호가 작을 수록 반지름이 크다.
ㄴ Tip. 단 2주기 원소인 Li 은 Na와 Mg를 제외한 3주기 원소들 보다 크다.
- 같은 족에서는 원자 번호가 클 수록 반지름이 크다.
3. 이온에서
- 같은 전자배치를 갖는 이온들은 원자 번호가 작을수록 반지름이 크다
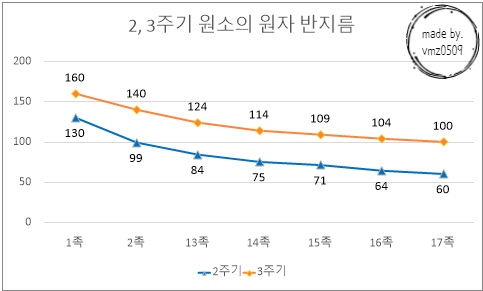
ㅇ 순차적 이온화 에너지
1. 제 1 이온화 에너지
: 기체 상태의 원자로부터 전자 1개를 떼어내는데 필요한 에너지
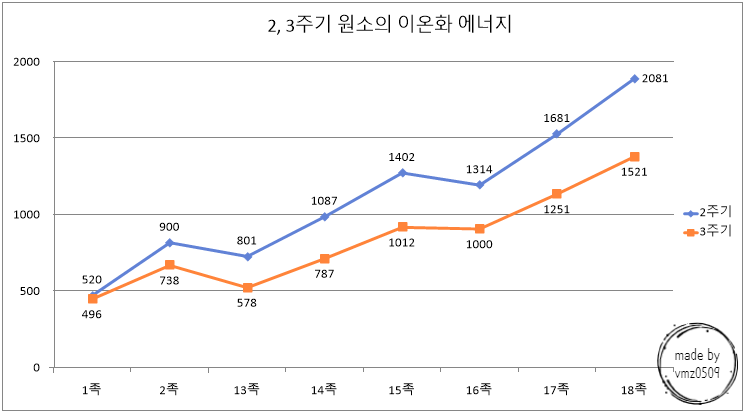
2, 3주기 원소의 이온화 에너지
2. 제 2 이온화 에너지
: 전자 1개를 떼어낸 원자의 이온에서 전자 1개를 추가로 떼어내는데 필요한 에너지
(위의 그래프에서 Li 자리에 Be을 쓰고, Ne 자리에 Na처럼 한 자리씩 당겨 쓰면 됨)
3. 제 3 이온화 에너지
: 전자 2개를 떼어낸 원자의 이온에서 전자 1개를 추가로 떼어내는데 필요한 에너지
(위의 그래프에서 Li 자리에 B를 쓰고, Ne 자리에 Mg처럼 두 자리씩 당겨 쓰면 됨)
'과탐 > 화학 1' 카테고리의 다른 글
| 화학 결합 ① - 이온 결합 (0) | 2022.09.07 |
|---|---|
| 2단원. 원자의 세계 요약정리 (0) | 2022.09.07 |
| 원자의 전자 배치 규칙 (0) | 2022.09.07 |
| 현대적 원자 모형(오비탈) (0) | 2022.09.07 |
